设计:随机对照观察实验。
时间及地点:于2011年6月至2012年6月在福建中医药大学中西医结合研究所完成。
材料:
实验动物:清洁级4周龄SD大鼠4只,10周龄SD大鼠40只,体质量250-300 g,由上海斯莱克实验动物有限责任公司提供,实验动物许可证号:SYXK(沪)2007-0005。实验过程中对动物的处置方法符合2009年《Ethical issues in animal experimentation》相关动物伦理学标准的条例。
实验方法:
桂枝加葛根汤含药血清制备:桂枝加葛根汤按《伤寒论》原方:葛根12 g,桂枝9 g,芍药9 g,生姜9 g,甘草6 g,大枣12枚,麻黄9 g,由福建中医药大学附属第二人民医院制剂中心一次性加工完成,制成含生药0.66 g/mL浓缩液,4 ℃保存备用。选用成年清洁级10周龄SD大鼠40只,按随机数字表法分为2组,分别为桂枝加葛根汤组和空白组,每组20只。根据人鼠用药量及体表面积换算得出灌胃量。2组灌胃方法如下:空白组以2 mL生理盐水灌胃;桂枝加葛根汤组以4 mL桂枝加葛根汤药液灌胃,每天1次,连续灌胃4 d。于末次灌胃2 h后乙醚吸入麻醉,于腹主动脉及心脏采血,3 000 r/min离心20 min,吸取上层血清,经56 ℃,水浴30 min灭活。用0.22 μm的微孔滤膜过滤除菌,置-20 ℃保存备用。
细胞干预培养液:空白组为含生理盐水SD大鼠血清15 mL加DMEM培养基85 mL;桂枝加葛根汤组为含桂枝加葛根汤SD大鼠血清15 mL加DMEM培养基85 mL。
大鼠纤维环细胞体外培养与传代[9]:4周龄SD大鼠称质量后脱颈处死,用体积分数75%乙醇浸泡5 min,常规铺巾,切取脊柱,切取纤维环,用无血清的DMEM液冲洗椎间盘纤维环,剪碎,并收集至无菌离心管。弃上清,于PBS中1 000 r/min离心5 min,洗涤2遍。加入含体积分数20%胎牛血清的DMEM培养液,将其吹打成单细胞悬液,接种到25 cm2细胞培养瓶,每瓶接种5 mL。接种细胞置37 ℃、体积分数5%CO2、95%湿度的恒温CO2培养箱中培养。3 d后首次全量换液,以后每3 d全量换液1次。12 d后原代细胞铺满瓶底,弃培养液,PBS洗涤2遍。每瓶加入0.25%的胰蛋白酶联合0.02% EDTA消化液2 mL,静置3-5 min。倒置显微镜观察,待细胞触角收缩变圆后,加入2 mL含体积分数为20%胎牛血清的DMEM培养液终止消化,移液器吹打成细胞悬浮液。移入离心管1 000 r/min离心5 min,弃上清,加入含体积分数为20%胎牛血清的DMEM培养液吹打均匀,以5×107 L-1的浓度接种到25 cm2一次性培养瓶中,每瓶接种5 mL。
将大鼠纤维环用眼科剪将组织剪成1 mm3组织块,再用PBS漂洗2遍,800 r/min×2 min离心,收集沉淀。用0.25%胰蛋白酶消化液重悬组织,37 ℃消化10-15 min,终止消化,800 r/min×2 min离心,去上清,沉淀用无血清培养液清洗2次;沉淀中加入0.1%Ⅱ型胶原酶37 ℃消化,待组织大部分消化、培养液浑浊后停止消化。1 000 r/min×5 min离心,收集沉淀。稀释细胞至1×108 L-1,接种细胞到100 mL塑料培养瓶中,生长培养液为DMEM(含体积分数10%胎牛血清、20 mmol/L HEPES,pH 7.2),置于37 ℃、饱和湿度、含体积分数5%CO2的孵箱中培养。倒置显微镜观察细胞生长情况,3 d换液1次。当细胞接近90%汇合时进行传代。弃掉培养液,用0.01 mol/L PBS洗涤细胞2次,弃掉液体。沿瓶壁加入数滴含0.25%胰蛋白酶和0.01%EDTA混合消化液,晃动培养瓶,镜下观察消化情况。镜下见细胞皱缩、间隙加大、个别细胞变圆漂浮时立即用含血清培养液3 mL终止消化;用滴管轻轻吹打细胞数次制成细胞悬液。悬液1 000 r/min×5 min离心,弃上清,培养液混悬细胞后按1∶2接种。传3代后进行以下实验。
纤维环细胞的鉴定:
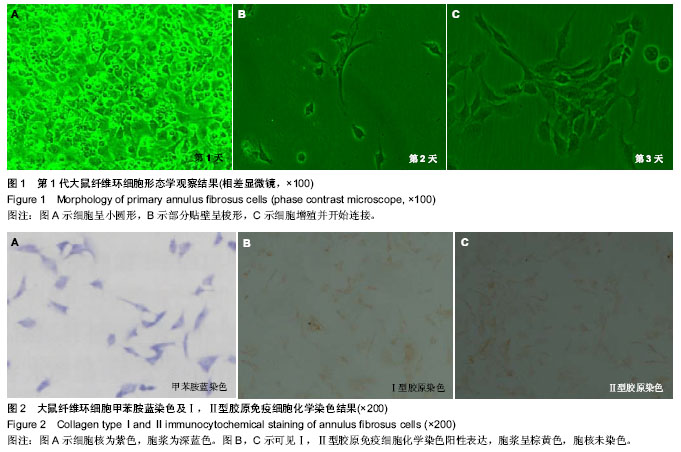
形态学鉴定:光镜观察细胞的形态。
纤维环细胞甲苯胺蓝染色:将传代细胞接种在放有预处理盖玻片的6孔培养板中进行细胞爬片,细胞爬片成功后,去除培养液,PBS冲洗3遍,40 g/L多聚甲醛室温固定 20 min;PBS冲洗,滴加甲苯胺蓝染液,室温30 min;自来水冲洗数秒;冰醋酸液分化数秒;蒸馏水洗2次,冷风吹干;二甲苯透明,中性树胶封固,显微镜下观察,拍照记录。
纤维环细胞Ⅰ型胶原、Ⅱ型胶原免疫细胞化学染色:将第3代传代纤维环细胞,以2×104/cm2接种在放有预处理盖玻片的6孔培养板中进行细胞爬片,爬片成功好,吸掉培养液,0.01 mol/L PBS(pH 7.4)洗涤2次;40 g/L多聚甲醛室温固定20 min;0.01 mol/L PBS(pH 7.4)洗涤,5 min×3次;体积分数3%双氧水室温30 min以封闭内源性过氧化物酶;0.01 mol/L PBS洗涤,5 min×3次;每片滴加正常山羊封闭血清30 μL,37 ℃孵育30 min;分别滴加Ⅰ型胶原单抗(1∶200稀释)、Ⅱ型胶原单抗(1∶200稀释),保湿状4 ℃过夜;阴性对照试验:以抗体稀释液代替一抗。滤纸吸掉多余一抗,0.01 mol/L PBS洗涤5 min×3次;加入二抗约400 μL,37 ℃孵育60 min;甩掉多余液体,0.01 mol/L PBS洗涤5 min×3次;加入SABC复合物适量,37 ℃ 20 min;0.01 mol/L PBS洗涤5 min×4次;加入数滴置的DAB(1 mL ddH2O依次加入A、B、C液各1滴,混匀),室温暗处显色,显微控制显色程度,约5 min,吸掉多余液体;自来水洗涤2次,甩掉多余液体;脱水、透明,中性树胶封固。显微镜下观察,拍照记录。
纤维环细胞药物干预:传3代纤维环细胞随机分为桂枝加葛根汤组和空白组。桂枝加葛根汤组分别加入含药血清的培养液(1 L培养基中含200 mL含药血清);空白组加入含生理盐水血清的培养液(1 L培养基中含200 mL含生理盐水血清)。置37 ℃、体积分数5%CO2、95%空气的CO2培养箱中干预6 d后,细胞达到70%-80%铺满瓶底时,用0.02%EDTA及0.25%胰蛋白酶联合消化,用含体积分数20%胎牛血清的DMEM培养液终止消化,1 000 r/min离心10 min,收集细胞。用10 mL PBS以1 000 r/min离心5 min,洗涤3次,细胞沉淀,反复冻融3次裂解,3 000 r/min离心10 min,收集上清液。
蛋白的提取:清空2组培养瓶中的培养基后,分别用4 ℃预冷的0.1 mol/L PBS洗涤3次,再将细胞小心刮下,转移至洁净1.5 mL离心管中,离心后弃去上清液。每管中加入200 μL 0.5 mol/L裂解液(7 mol/L尿素,2 mol/L硫脲,0.1%PMSF,65 mmol/L DTT),超声波破碎仪处理(超声条件:常规的人或者小鼠细胞超声70-75 W,超声5 s停10 s,超声3-5次),冰上放置40 min,低温高速离心 (14 000 r/min,4 ℃离心30 min)后,取上清液。用bradford方法测定各组蛋白的浓度后,-80 ℃保存备用。
同位素标记相对和绝对定量技术标记:取2组样品各100 μg进行如下处理:每管各加入预冷的丙酮(丙酮∶样品体积比=5∶1),-20 ℃沉淀1 h。12 000 r/min离心15 min,弃上清,用试剂盒中自带的溶解液(20 μL)和1%SDS(1 μL)充分混悬溶解样品。加入还原试剂2 μL,60 ℃反应60 min。加入半胱氨酸封闭试剂1 μL,室温处理10 min。按照酶∶蛋白质=1∶20的比例加入胰蛋白酶,37 ℃酶解过夜。113,118,119各管标记试剂中加入50 μL异丙醇(试剂盒中自带),混匀,分别加入各管样品中,室温反应1 h,之后各加入3倍体积水,使标记试剂分解。标记和样品对应关系如下:空白组(IT118)、桂枝加葛根汤组(IT115)。合并各管标记好的样品,真空冷冻干燥。
脱盐:采用Sep-Pak Vac C18小柱脱盐。即将标记过程中的标记试剂和相关buffer的盐,以便于后续分析。 ①100%乙腈冲洗柱子3次。②0.1%TFA (水溶),冲洗柱子3次。③用400 μL 0.1%TFA溶解样品,加载到柱子上。 ④0.1%TFA冲洗柱子3-5次。⑤用50%乙腈0.1%TFA 400 μL洗脱下样品。将样品冷冻干燥后进行后续分析。
第一维强阳离子柱(SCX)分离:第一维强阳离子柱分离:流动相A液含10 mmol/L KH2PO4和25%ACN,pH 2.6;B液含10 mmol/L KH2PO4、350 mmol/L KCl和25%ACN,pH 2.6。将冻干样品溶解于80 μL A液并全部上样。设紫外检测波长为214 nm/280 nm,流速为200 μL/min。线性梯度洗脱程序为:5-40 min,5%-25%B;40-45 min,25%-80%B;45-50 min,80%B;50-60 min,0%B。根据峰形和时间共收取20个梯度,真空离心浓缩后,每馏分用50 μL反相液相色谱的A相溶解,进样量20 μL。进行第二维分析。
第二维反相液质联用RPLC-MS:第二维反相液相色谱:流动相A液为体积分数为5%乙腈和0.1%甲酸溶液,流动相B液为体积分数为95%乙腈和0.1%甲酸溶液。流速:300 nL/min。RPLC柱线性梯度洗脱程序为:0-5 min,上样;5-90 min,5%-35%B;90-95 min,35%-80%B;95-100 min,80%B;100-105 min,80%-5%B;1 200 min停止。
质谱鉴定:纳喷雾针直接连接于反相色谱柱末端作为喷雾接口,喷雾电压2.2 kV。MS扫描范围400-1 800 U,一个谱图选择4个最强的母离子进行串级扫描,MS/MS扫描范围100-2 000 U。
数据库搜索:所得串级质谱分析数据用Protein Pilot 3.0对IPIv 3.45 mouse数据库进行检索,得到肽段和蛋白质鉴定信息,种属选择是大鼠,根据软件对鉴定到的蛋白质打分,对应蛋白质的假阳性率为5%。软件依据同位素报告基团的相对含量进行蛋白质定量,以空白组为对照,选择差异显著(P ≤ 0.05)的结果报告。实验采用2为标准差为有意义。所以蛋白平均比值大于2或小于0.5被认为有明显表达改变。
主要观察指标:运用同位素标记相对和绝对定量技术标记2组样本的蛋白,二维液相色谱质谱仪(2D LC-MS/MS)鉴定蛋白并进行相对定量分析。

.jpg)